A világ élvonalába tartozik, de Magyarországon dolgozik Győrffy Balázs, a Semmelweis Egyetem tanszékvezetője, a Pécsi Tudományegyetem intézetigazgatója, a HUN-REN TTK kutatócsoport vezetője, az egyik legtöbbet hivatkozott hazánkban dolgozó kutató. Számos konkrét gyógyszer kifejlesztésében is segítséget jelentő munkájáról kérdeztük.

A „Highly Cited Researchers” (Leggyakrabban hivatkozott kutatók) elnevezés egy olyan listát jelöl, amelyet a Clarivate cég évente tesz közzé a világ kutatóinak mintegy 0,1 százalékáról, akiknek a munkáira a legtöbbet hivatkoznak. A magyar tudósok között ide tartozik a Nobel-díjas Karikó Katalin is. Győrffy Balázsnak az interjú készítésének időpontjában 39 508 hivatkozása volt. Ezen mutató szerint Magyarország nem teljesít túl jól: az idei listán Győrffy Balázs az egyetlen itthon dolgozó kutató, tavaly kettő, tavalyelőtt három, az előtte lévő évben négy kutató szerepelt a listán. A régiónkban lévő, szomszédos országoknak jobbak a mutatói: Csehországban például hét ilyen kutató is dolgozik. A 6 millió fős lakosságú Szingapúrban 86 Highly Cited kutató dolgozik.
Kezdjük azzal: hogyan alakul ki a rákos daganat?
Az emberi szervezet sejtjeinek genetikai állományában egymás után több mutáció alakulhat ki. Hat olyan jellemző van, aminek mindenképpen meg kell jelennie ahhoz, hogy rákos daganat jöhessen létre. Van egy nagyobb lista is, de ezek közül hat a legfontosabb. Az első, hogy beinduljon az állandó osztódás. A sejtekben vannak daganat elleni védelmi rendszerek, amelyek elnyomják a tumorokat. A második jellemző, hogy ezeket a tumornak ki kell tudnia kapcsolnia. Az egészséges szövetben a sejtek egy idő után maguktól sejthalálba, apoptózisba kerülnek. A harmadik jellemző, hogy a daganatnak ezt ki kell tudnia kerülnie és el kell érnie az osztódási halhatatlanságot, tehát az állandó osztódást. A sejtosztódás során van egy védősapka a kromoszómák végén, és ebből a védősapkából minden egyes osztódáskor levágódik egy pici darab. Körülbelül olyan 30-35 osztódás után ez a sapka elfogy, és utána nem tud a sejt tovább osztódni. A tumoroknak aktiválniuk kell egy enzimet, ami ezt a képességet visszaépíti, különben nem tudnak továbbosztódni. Ez a negyedik feltétel. Végül az ötödik, hogy a sejtosztódás során az új erek képződésének kell aktiválódniuk, mert ugye, ha ez nem aktiválódik, akkor egy idő után nem lesz elegendő tápanyag és oxigén, a tumor elpusztul. Az utolsó és legfontosabb jellemző, hogy el kell érnie azt, hogy képes legyen invázióra és áttétképzésre.
Ilyenkor egy tumorsejt leszakad, a keringésen vagy a nyirok keringésen át eljut a szervezetnek egy távolabbi pontjára, ott megtelepszik, és ott újra osztódni kezd.
Az lesz az áttét.
A betegek halálát szinte mindig az áttétek okozzák. A tumort onnantól nevezzük rosszindulatúnak, amikor áttétet alkot. Mindaddig, amíg egy tumor nem ad áttétet, hanem csak egy helyen van, sebészileg el lehet távolítani, és ilyenkor jóindulatú tumorról beszélünk. Rendkívül érdekes folyamat, amit egyébként az onkológusok nagy része sem tud, hogy hogyan kezdődik ez az áttétképzés. Nagyon-nagyon sok tumoros sejt van és időnként leszakadnak sejtek, amik elindulnak a keringésben, és körbe mennek. De ugye mindenütt ellenséges számukra a szervezet, mindenütt ott van az immunrendszer, más a kémhatás, szóval egymillió problémával találkoznak. Ezért van az, hogy a tumorsejteknek csak egy nagyon pici része jut vissza a daganatba, és ott újra megtelepszik. A körforgáson keresztül a tumorba tehát mindig visszajutnak olyan sejtek, amik már megjárták a keringést, és az azt jelenti, hogy a tumorban lévő sejtek egyre ellenállóbbak lesznek, és egy idő után eljutnak odáig, hogy az a sejt, ami leszakad, az már meg tud telepedni egy távoli szervben is.
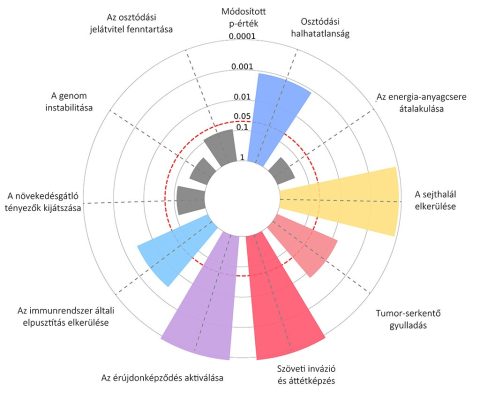
Forrás: cancerhallmarks.com
A kemoterápiánál hússzor jobb
Milyen mechanizmusokon alapul a rosszindulatú daganatok kezelése?
Amikor már áttétek keletkeznek, akkor már nincs értelme a sebészetnek, de van a két jól ismert további lehetőség, amivel a tumorokat kezelni lehet: a radioterápia, illetve a gyógyszeres terápia. A radioterápia lényege, hogy besugározzuk a tumorsejteket, ahol genetikai hibák keletkeznek, majd bizonyos enzimek felismerik ezeket a genetikai hibákat, és sejthalálba viszik a sejtet. A gyógyszeres kezeléseknél viszont egy gigászi armada áll jelenleg rendelkezésre.
Mivel foglalkoznak önök a kutatásaik során?
A hagyományos gyógyszeres terápia lényege, hogy a rákos sejtet az különbözteti meg a normál testi sejtektől, hogy a rákos sejtek folyamatosan osztódnak. Tehát hogyha az összes osztódó sejtet elpusztítjuk a szervezetben, akkor a tumort is el fogjuk pusztítani. Ez a kemoterápiás kezeléseknek az alapja.
Ezzel az a probléma, hogy nagyon sok olyan szerv van, amiben nagyon intenzív sejtosztódás zajlik, mint például a haj, a belek és a csontvelő. A kemoterápia pedig az egészséges sejteket is elpusztítja. Tehát kihullik a betegnek a haja, a belekben lévő intenzív sejtosztódás miatt lesz hasmenésük, ezért lesznek vérszegények, és emiatt megy tönkre az immunrendszerük, mert a csontvelőben lévő sejtosztódást is gátoljuk.
Az elmúlt 25 év alatt jelentek meg azok a célzott terápiás kezelések, ahol egy olyan jellemzőjét próbáljuk a daganatnak megcélozni, amely a normál sejtekben nincsen jelen.
Ez azt eredményezi, hogy egy ilyen kezelés jóval kevesebb mellékhatással fog járni. A legelső ilyen a hormonterápia volt, ez már a ’70-es években megjelent, és a ’80-as években terjedt el. Ennek az a lényege, hogy egyes tumorsejtek a hormonok hatására jobban növekednek.
Ha ezt a hormonhatást blokkoljuk, akkor a tumornak a növekedése is megáll. A mi kutatási területeinknek az egyik fókusza az emlő tumora, ahonnan egy jó példát tudok bemutatni.
A ’80-as, ’90-es években találták meg a HER2 gént. Azt figyelték meg, hogy ahol a HER2 gén aktívabban működik, azoknak a betegeknek sokkal rosszabb a kilátása. A ’90-es évek során készítettek egy gyógyszert, a HER2 gén fehérjeterméke ellen. Tehát ez egy „HER2 ellenes célzott terápia” azokra a tumorokra, amelyek HER2 pozitívak.
Ez azt jelenti, hogy immunhisztokémiai módszerrel megfestik a tumort, és megnézik, hogy ott vannak-e ezek a fehérjék. Ha a sejtek felszínén jelen van ez a fehérje, nagyon jól látszik, mert a sejtek széle elszíneződik. Ilyenkor érdemes HER2-ellenes terápiát adni. Olyan jól „bejött” ez a kezelés, hogy a HER2-ellenes terápiának a hatékonysága a hagyományos kemoterápia hatékonyságának a hússzorosa lett. És az lett a végeredmény, hogy ma egy HER2 pozitív tumornak sokkal jobb a prognózisa, mint egy HER2 negatívnak. Van többféle ilyen kezelés, és akkor itt beszélnék arról, amit a mi kutatásainkban csinálunk.
A Google Scholar szerint kiemelkedően sok, 3076 hivatkozás érkezett az Önök cikkére, amely a Breast cancer research and treatment (magyarul: Az emlőrák kutatása és kezelése) folyóiratban jelent meg. Mi a lényege a kutatásnak? Mi a célja az Önök által kifejlesztett KM plot rendszernek?
Az volt az ötletünk, hogy miért nézzük a géneket egyesével, mikor az összes gént egyszerre is tudnánk vizsgálni. Megnézzük, hogy hogyan függ össze a gének aktivitása a betegség kilátásával. Amit mi csináltunk, és ami ebben a cikkben is benne van, hogy megnéztük különböző tumortípusokban, hogy melyek azok a legjobb terápiás célpontok, amelyek a jövő gyógyszereinek a célpontjai lehetnek. Nagyon sokan idézték ezt a cikket, azaz sok más kutatás tudta használni az eredményeinket, mert egyrészt gyors online elemzést ad a kutatóknak, másrészt segít új gyógyszercélpontok és biomarkerek azonosításában. Más tumorokban is végeztünk hasonló vizsgálatot és ezeknek az eredményeként ma már több mint négyszáz szabadalom van, ami a cikkeinket idézi. A szabadalmakat nem mi nyújtottuk be, hanem gyógyszercégek, és kutatóintézetek a világon mindenfelé. Ez azt jelenti, hogy nagyon sokan használták fel mások a mi munkánkat arra, hogy új gyógyszeres kezeléseket tudjanak fejleszteni.
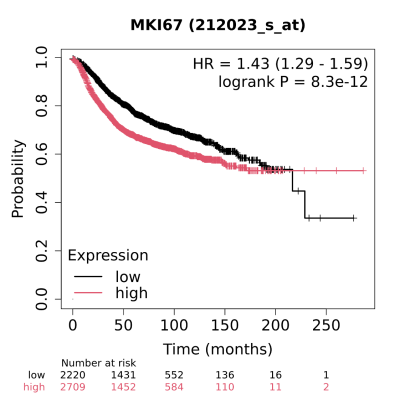
Forrás: kmplot.com
Több tízezer beteg adataiból lehet megbecsülni a kilátásokat
Mindezt az tette lehetővé, hogy leolvasták sok ember genetikai állományát, vagy pedig a rákos sejtek genetikáját elemzik?
Az onkolóiai kutatásnak van egy rossz oldala: az, hogy ez egy nagyon súlyos betegség. De a kutatásnak van egy olyan vonatkozása is, hogy nagyon sok tumort megműtenek.
Ez azt jelenti, hogy a tumor kikerül a betegekből, és így lesz egy szövetmassza, amit meg lehet vizsgálni, hogy mi a csuda is volt ez a rossz indulatú dolog. Már temérdek tumort megvizsgáltak, és ezeket az eredményeket nagyon-nagyon sokan leközölték. Mi magunk is készítettünk ilyet, és mások is végeztek ilyen vizsgálatokat. Ezután összeszedtük a mások által mért paramétereket: minden egyes gén kifejeződését a tumorokban, és így tudjuk, hogy mi történt a betegekkel. Már több mint 15 éve folytatjuk ezeket a fejlesztéseket és a több tízezer beteg így összegyűjtött adatai alapján sok tumor típusnál meg tudjuk mondani, melyek azok a gének, amelyek összefüggenek azzal, hogy a betegnek jók, vagy rosszak lesznek a kilátásai. Mindegyik gén, amelyiknek kifejeződése jelentősebb azokban, akiknek rossz lesz a kilátása, alkalmas terápiás célpont lehet.
Mit tud tenni az ember a hétköznapokban, hogy csökkentse egy daganatos betegség kockázatát?
Most nyilván ne beszéljünk olyan általánosságokról, hogy ne cigarettázzon. Ezen nincs értelme gondolkodni, mert a cigaretta önmagában is nagyon sok tumornak megnöveli a rizikóját.
De van néhány dolog, amit szerintem érdemes mindenkinek fejben tartani. Vannak ajánlások, hogy mik azok az anyagok, amelyek kifejezetten rákkeltőek. Ilyen például az azbeszt, amit mára be is tiltották.
Egy másik, sokkal kevésbé ismert anyag, a nátrium-nitritek csoportja, amelyekkel a húst tartósítják. Ha bemegyünk akármelyik élelmiszerboltba, szinte az összes tartósított és feldolgozott húsáru, ami nem nyers hús, az nálunk nátrium-nitrittel van tartósítva. Az Amerikai Rákkutató Társaság (American Association for Cancer Research, AACR, https://www.aacr.org/ ) lassan egy évtizede besorolta, hogy ez egy I. kategóriájú karcinogén, ami ugyanaz a kategória, mint a cigaretta. Számomra őszintén döbbenetes, hogy Magyarországon alig terjedt el, hogy nátrium nitrit mentes húsokat is lehessen kapni a boltban, pedig csak ilyet lenne szabad az embereknek fogyasztaniuk.
Ha valaki egy hibát örököl a hatból
Mi a helyzet a genetikával?
Vannak a fentebb említett környezeti faktorok, emellett természetesen a genetikai tényezők is szerepet játszanak. Lehet valakinek olyan genetikai hibája, aminek alapján bizonyos tumoroknak megnő a valószínűsége. Erre ma már vannak genetikai szűrővizsgálatok, amivel meg lehet valakiben vizsgálni egyszerre az összes ilyen gént. Tudjuk, hogy pontosan mely géneket érdemes megnézni. Korábban említettem a genetikai hibákat. Mi van, ha valaki egy génhibát örökölt a hatból? Ha nála az egyik gén már eleve hibás? Ez azt jelenti, hogy neki már csak öt mutációra van szüksége, hogy létrejöjjön a tumor. Vannak már genetikai szűrővizsgálatok, amelyekkel ezeket lehet megállapítani.
Érdemes szűrővizsgálatokra járni?
A szűrővizsgálatok egy egészen nagy és komplex területet képeznek. Bizonyos tumor típusokra vannak tesztek: a tüdőrákra, az emlőrákra, a vastagbélrákra, a prosztatatumorra és a méhnyakrákra. Érdemes mindenkinek megnéznie, milyen életkorban milyen tesztre érdemes mennie.